Причини, імунологічні механізми та сучасне лікування в нейроофтальмології
Авторка Наталія МОЙСЕЄНКО, д. мед. н., доцент, завідувачка кафедри офтальмології ІФНМУ, лікар-нейроофтальмолог
Вступ
Атрофія зорового нерва — це серйозне захворювання, при якому відбувається загибель аксонів зорового нерва з подальшим заміщенням нервової тканини гліозною та сполучною. Найчастіше атрофія зорового нерва розвивається як наслідок гострої або рецидивуючої оптичної невропатії (запальної оптичної невропатії). У сучасній нейроофтальмології (2026 рік) ми розуміємо, що імунологічні механізми — аутоімунні процеси — є провідними причинами прогресуючої атрофії зорового нерва у молодих та середнього віку пацієнтів. Рання серологічна діагностика та таргетне лікування дозволяють зберегти зір навіть у випадках, які раніше вважалися невиліковними.
Причини атрофії зорового нерва: імунологічний акцент
Класичні причини атрофії зорового нерва включають ішемію (передня ішемічна оптична невропатія, глаукома), компресію (пухлини орбіти), токсини та спадкові захворювання (LHON). Однак у 2025–2026 роках лідирують аутоімунні та запальні оптичні невропатії:
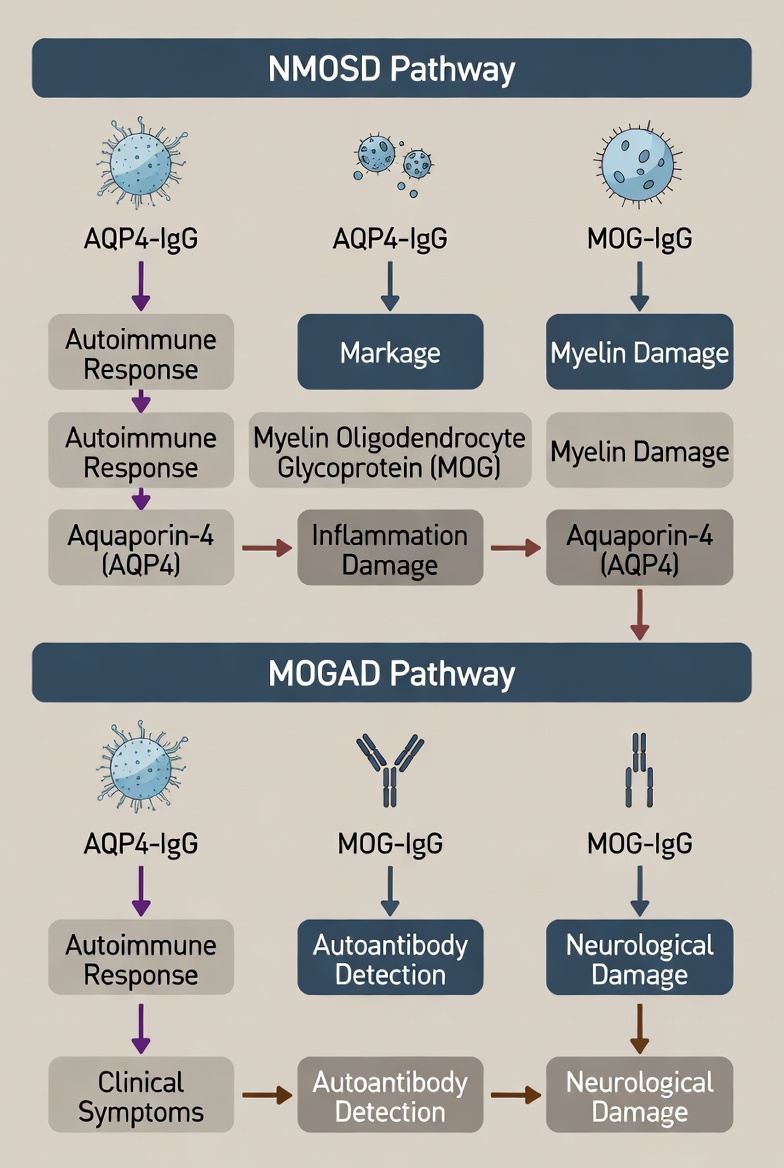
- NMOSD (нейромієліт оптика спектра, AQP4-асоційований)
- Антитіла до аквапорину-4 (AQP4-IgG) викликають комплемент-опосередковане запалення астроцитів зорового нерва → некроз аксонів → швидка атрофія зорового нерва. Без специфічної імуносупресії (ритуксимаб, екулізумаб, інаебілізумаб, телітлізумаб) ризик сліпоти на око сягає 60–80% за 5 років. Раннє виявлення AQP4-IgG дозволяє зупинити рецидиви та зберегти зір.
- MOGAD (MOG-асоційоване захворювання)
- Антитіла до мієліну олігодендроцитів глікопротеїну (MOG-IgG) провокують демієлінізацію та аксональне пошкодження. Характерно двобічний папіліт з вираженим набряком, кращий регрес після першої атаки, але рецидиви призводять до накопичення атрофії зорового нерва. Прогноз кращий, ніж у NMOSD, — часто >80% пацієнтів відновлюють високий зір при своєчасній імуносупресії (азатіоприн, мікофенолат, ритуксимаб).
- Серонегативні та overlap-форми аутоімунної оптичної невропатії
- Системний червоний вовчак, синдром Шегрена, саркоїдоз (нейросаркоїдоз), IgG4-асоційована хвороба, тиреоїд-асоційована оптична невропатія → хронічне гранульоматозне або васкулітне ураження → вторинна атрофія зорового нерва. Тут ключові маркери: ANA, ACE, lysozyme, IgG4, тиреоїдні антитіла.
- Хронічна імунна активація
- Навіть без специфічних антитіл мікроглія, Th17-клітини та комплемент призводять до аксональної дегенерації. Це пояснює прогрес атрофії в “ідіопатичних” випадках без довготривалої імуномодуляції.
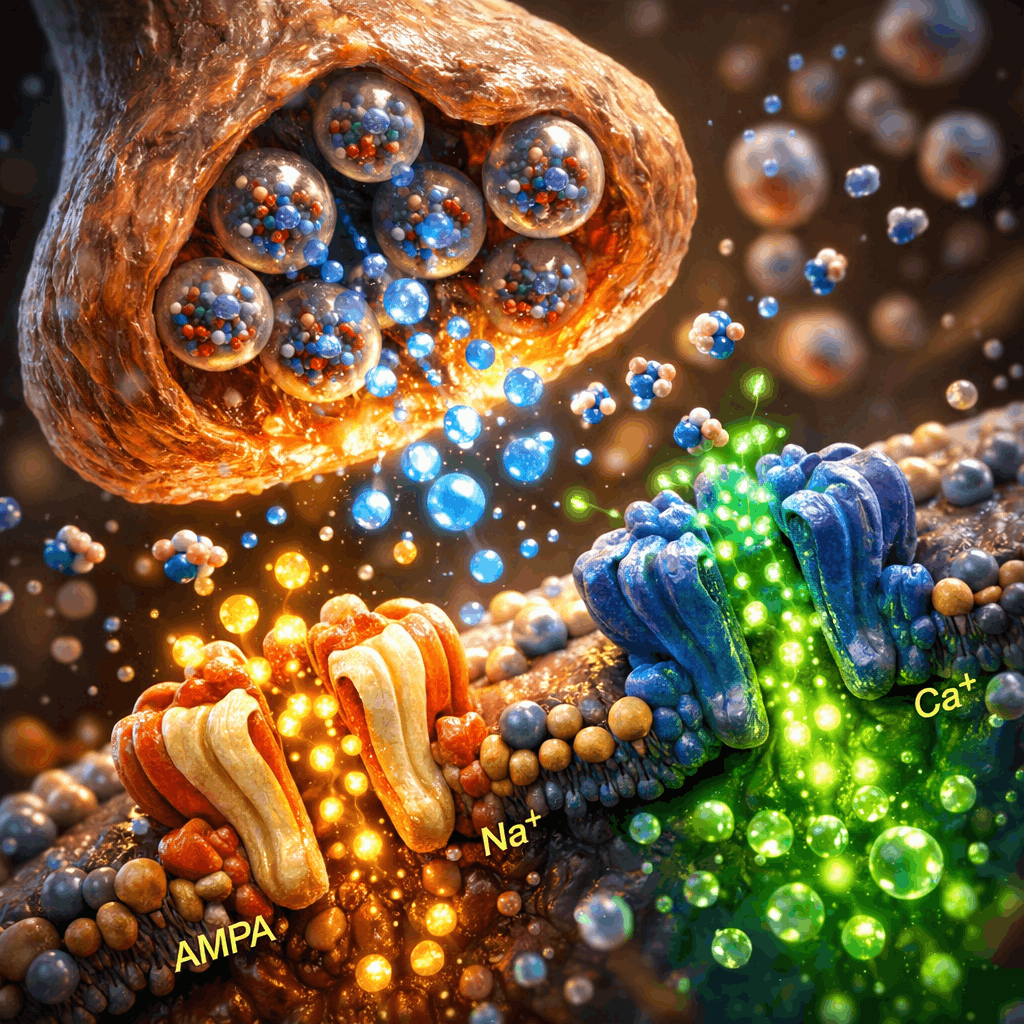
Чому рання діагностика змінює прогноз атрофії зорового нерва?
Раніше атрофія зорового нерва часто вважалася кінцевою стадією без шансів на відновлення. Сьогодні серологічна діагностика (AQP4-IgG, MOG-IgG, NfL, sGFAP) + ОКТ + МРТ дозволяють втрутитися на етапі запалення:
- Позитивний AQP4-IgG → негайна профілактика рецидивів → ризик сліпоти падає до <20%.
- MOG-IgG → персоналізована терапія → високий шанс збереження зору.
- Розширена панель (ANA, IgG4, тиреоїдні маркери, ACE) → точне визначення причини в складних випадках.
Діагностика атрофії зорового нерва: особливості серологічного тестування
Щоб точно встановити причину запальної оптичної невропатії та запобігти атрофії зорового нерва, ключовими є серологічні маркери — антитіла AQP4-IgG (для NMOSD) та MOG-IgG (для MOGAD). Але ці тести — не прості аналізи крові. Вони вимагають спеціальних умов, високоточної методики та досвіду лабораторії, тому не кожна установа в Україні здатна забезпечити надійний результат.
Чому не кожна лабораторія може якісно виявити AQP4-IgG та MOG-IgG?
Ці антитіла розпізнають конформаційні епітопи (нативну, “живу” структуру білків аквапорину-4 та мієліну олігодендроцитів глікопротеїну). Тому золотий стандарт — live cell-based assay (живий CBA) або високоякісний fixed CBA з використанням flow cytometry (FACS) чи immunofluorescence (IFT).
- Звичайні ELISA або старі методи часто дають хибнонегативні результати (чутливість падає до 45–70% проти 95–97% у live CBA).
- Потрібні спеціально трансфектовані клітини (HEK-293 з людським MOG або AQP4), точний контроль якості, кваліфіковані лаборанти та стандартизована інтерпретація (титри ≥1:100–1:200 для MOG-IgG, ≥1:20 для AQP4-IgG вважаються позитивними).
- У 2025–2026 роках live CBA перевершує fixed за чутливістю (95–97% vs 45–72% для MOG-IgG), тому фіксовані тести можуть пропускати випадки MOGAD або NMOSD.
В Україні такі аналізи доступні в обмеженій кількості лабораторій (наприклад, SmartLab, Esculab, деякі великі центри з відправкою зразків за кордон для FACS). Не кожна регіональна лабораторія має обладнання та сертифікацію для cell-based assay — тому часто доводиться відправляти кров до Києва чи за межі країни.
Який біоматеріал потрібен: кров чи спинномозкова пункція
- Сироватка крові (венозна кров) — основний і найбільш чутливий матеріал. Для AQP4-IgG сироватка майже завжди краща (чутливість вища, ніж у лікворі; CSF-позитивні пацієнти зазвичай мають високий титр у крові). Для MOG-IgG сироватка теж переважає (концентрація в крові вища), але в рідкісних випадках (3–5%) буває CSF-restricted MOG-IgG (тільки в лікворі). Рекомендація: починати з аналізу крові на AQP4-IgG + MOG-IgG (IFT або CBA).
- Спинномозкова пункція (ліквор, CSF) — потрібна в окремих випадках
- При негативному результаті в крові, але високій клінічній підозрі на MOGAD (атиповий перебіг, кортикальний енцефаліт, рецидивуючий мієліт).
- Для оцінки інтратекального синтезу (підвищений antibody index).
- Додатково для біомаркерів пошкодження (NfL, sGFAP у лікворі).
- Для AQP4-IgG пункція рідко додає цінності (CSF-позитивні майже завжди мають позитив у сироватці). Пункцію роблять тільки за суворими показаннями: ризик ускладнень, потреба в анестезіолога/невролога. Ангіографія для оцінки судинних аномалій.
Практичні рекомендації для пацієнтів та лікарів
- Здавайте кров на AQP4-IgG та MOG-IgG якомога раніше (до або на початку пульс-терапії стероїдами — високі дози можуть тимчасово знизити титр).
- Оберіть лабораторію з cell-based assay (live CBA або якісний IFT/FACS) — це запорука точності.
- Якщо результат негативний, але клініка атипова — розгляньте повтор або аналіз ліквору (спинномозкова пункція).
- У Івано-Франківську та регіоні можлива консультація з направленням на тестування в сертифіковані лабораторії.
Що робити, якщо тест на AQP4-IgG або MOG-IgG виявився позитивним?
Позитивний результат серологічного тесту (AQP4-IgG або MOG-IgG) — це не вирок, а ключ до точного діагнозу та ефективного контролю захворювання. Багато пацієнтів, почувши “NMOSD” чи “MOGAD”, лякаються, бо раніше ці стани асоціювалися з швидкою втратою зору чи інвалідизацією. Сьогодні ситуація кардинально інша: раннє виявлення маркера розв’язує нам руки для персоналізованої терапії, яка запобігає рецидивам і зберігає зір у більшості випадків.
Чому не варто панікувати при позитивному результаті?
- Це не “рак” чи невиліковна хвороба — NMOSD та MOGAD — хронічні аутоімунні стани, але з високоефективними методами контролю. З появою таргетних препаратів (моноклональних антитіл) ризик сліпоти суттєво знизився.
- Позитивний тест — це перевага: ми знаємо точну причину запалення зорового нерва, а не лікуємо “навмання”. Це дозволяє перейти від симптоматичної терапії до профілактики рецидивів уже після першої атаки.
- Прогноз значно кращий при ранньому втручанні: за сучасними даними (2025–2026 рр.), при своєчасній імуносупресії ризик повторних атак падає до 10–20% за 5–8 років у багатьох пацієнтів, а зір зберігається або відновлюється на високому рівні.
Що ми робимо при позитивному AQP4-IgG (NMOSD)?
- Гостра атака: високодозові кортикостероїди (метилпреднізолон 1 г/добу 3–5 днів) + плазмаферез або імуноадсорбція, якщо ефект слабкий.
- Профілактика рецидивів (must-have після першої атаки):
- Перша лінія — ритуксимаб (анти-CD20, деплеція B-клітин) — найчастіше використовується в Україні та світі через доступність і доведену ефективність.
- Таргетні препарати: інебілізумаб (анти-CD19), сатралізумаб (анти-IL-6), екулізумаб/равулізумаб (інгібітори комплементу) — особливо при тяжких атаках або непереносимості ритуксимабу.
- Моніторинг:
- регулярні аналізи на титр AQP4-IgG (динаміка), NfL/sGFAP (як біомаркери пошкодження), + ОКТ (товщина шару гангліозних клітин та перипапілярного шару нервових волокон), периметрія (візуальні поля), оцінка зіничних реакцій та гостроти зору.
Що при позитивному MOG-IgG (MOGAD)?
- Гостра атака: ті ж високодозові стероїди, часто з кращим відновленням зору, ніж у NMOSD.
- Профілактика рецидивів рішення індивідуальне. У багатьох випадках після першої атаки можна обмежитися повільним відміною стероїдів. Але при тяжкій атаці, рецидиві або стійкому високому титрі MOG-IgG — призначаємо імуносупресію: азатіоприн, мікофенолат мофетил, ритуксимаб (особливо при вищій інвалідності). Таргетні препарати (наприклад, сатралізумаб) тестуються в клінічних дослідженнях.
- Моніторинг: динаміка титру MOG-IgG (зниження часто корелює з ремісією), ОКТ (чутливий до субклінічного пошкодження), периметрія, NfL.
Динамічний моніторинг: чому це важливо при хронічних станах
NMOSD та MOGAD — хронічні захворювання, тому лікування не “один раз і назавжди”. Ми оцінюємо:
- Зміни лабораторних показників (титри антитіл, NfL як маркер аксонального пошкодження).
- Стан зорового нерва: ОКТ (раннє виявлення витончення шару гангліозних клітин навіть при нормальній гостроті зору), периметрія (виявлення дефектів полів зору), зіничні реакції (афферентний дефект зорового нерва), кольоровий зір.
Це дозволяє вчасно коригувати терапію: посилювати при підвищенні титру чи субклінічному прогресі, або деескалювати при стабільній ремісії (особливо в MOGAD).
Щодо МРТ: неоднозначна картина
МРТ орбіт та головного/спинного мозку — важливе, але не завжди корелює з серологією:
- Може бути позитивний AQP4-IgG або MOG-IgG при “нормальному” МРТ (особливо в ізольованому оптиконевриті без типового довгого ураження).
- Навпаки — вогнища на МРТ (ураження зорового нерва, спинного мозку) можуть бути при серонегативних формах або інших причинах.оширення запального процесу:
- Тому МРТ — це “де і як” уражено, а серологія — “чому”. Вони доповнюють один одного, але саме позитивний маркер визначає стратегію лікування.торинні ефекти:
Роль нейроофтальмолога в діагностиці та лікуванні оптичних невропатій з позитивними імунологічними маркерами (NMOSD, MOGAD та іншими)
При позитивному результаті на AQP4-IgG, MOG-IgG чи інших імунологічних маркерах саме нейроофтальмолог стає головним фахівцем, який поєднує глибокі знання неврології та офтальмології. Звичайний офтальмолог, навіть дуже досвідчений, найчастіше просто не стикається з цими рідкісними аутоімунними станами в повсякденній практиці і може не знати сучасних нюансів серологічної діагностики та таргетної терапії. Невролог, який лікує основне захворювання (розсіяний склероз, саркоїдоз чи системний червоний вовчак), чудово працює з мозком і спинним мозком, але рідко має час і обладнання для щоденного моніторингу саме зорового нерва — тонкощів його структури, динаміки атрофії та функціонального стану.
Чому саме нейроофтальмолог?
- Точна інтерпретація «очних» проявів імунного процесу Ми бачимо те, чого не помітить ні звичайний офтальмолог, ні невролог:
- раннє витончення шару гангліозних клітин та нервових волокон на ОКТ (навіть коли гострота зору ще 1,0);
- субклінічні дефекти полів зору на периметрії;
- зміни зіничних реакцій (відносний аферентний дефект);
- динаміку набряку диска та переходу в атрофію.
- Координація лікування з урахуванням зору як головного критерію успіху
- Коли маркер позитивний, ми не просто призначаємо ритуксимаб чи інаебілізумаб — ми щомісяця або кожні 3 місяці оцінюємо, чи захищає ця терапія саме зоровий нерв. Якщо титр антитіл падає, а на ОКТ товщина шару стабільна — можемо говорити про хорошу відповідь. Якщо з’являється субклінічне витончення — коригуємо схему раніше, ніж настане чергова атака.
- Моніторинг у динаміці — наша головна перевага NMOSD і MOGAD — хронічні захворювання. Ми ведемо пацієнта роками:
- серологічний контроль (титри AQP4/MOG, NfL/sGFAP);
- структурний контроль (ОКТ кожні 3–6 місяців);
- функціональний контроль (периметрія, контрастна чутливість, кольоровий зір). Саме цей комплекс дозволяє вчасно помітити загрозу атрофії зорового нерва і не допустити її.
- Мультидисциплінарна координація
- Ми працюємо в тісному контакті з неврологом-імунологом, ревматологом, ендокринологом, але саме нейроофтальмолог є «охоронцем зору» — тим, хто каже: «Терапія ефективна для мозку, але зір починає страждати — потрібно посилити або змінити препарат».
Висновок
Якщо у вас або ваших близьких виявили позитивний AQP4-IgG чи MOG-IgG — не панікуйте і не затягуйте з візитом саме до нейроофтальмолога. Звичайний офтальмолог може сказати «все добре, диск блідий, але зір нормальний», а невролог — «приймайте таблетки, головне — мозок». Тільки нейроофтальмолог поєднує обидва світи і робить так, щоб зір залишався на максимально можливому рівні протягом усього життя.
У клініці Люкс Віжн (Івано-Франківськ) я веду таких пацієнтів за сучасними міжнародними протоколами 2026 року: від першої інтерпретації аналізів до багаторічного моніторингу ОКТ і підбору імуносупресії. Це дозволяє більшості пацієнтів з NMOSD і MOGAD жити без рецидивів і зберігати високий зір.
Звертайтесь одразу після отримання позитивного результату — чим раніше ми візьмемо процес під контроль, тим кращий буде результат.
Я — лікар нейроофтальмолог, Івано-Франківськ, клініка Люкс Віжн. Для запису на консультацію звертайтесь на рецепцію клініки.
Рекомендовані джерела літератури
Для NMOSD та AQP4-IgG
- Yang WYO et al. (2025). Neuromyelitis optica spectrum disorder (NMOSD): Recent advances and insights from Taiwan. Journal of the Formosan Medical Association. DOI: 10.1016/j.jfma.2025.XX (огляд діагностики, лікування та рецидивів у AQP4+ NMOSD, акцент на моноклональні антитіла).
- Chaitanuwong P et al. (2025). Optic neuritis: a comprehensive review of current therapies and emerging treatment strategies. Frontiers in Neurology. PMC12214357 (порівняння терапії ON при MS, NMOSD та MOGAD, з акцентом на AQP4-IgG та таргетні препарати: екулізумаб, інебілізумаб, сатралізумаб).
- Yamaguchi C et al. (2025). Differentiation of acute-phase AQP4-IgG+ optic neuritis from CNS inflammatory diseases using optic nerve head blood flow analysis. Scientific Reports, 15:33618. DOI: 10.1038/s41598-025-19110-7 (використання OCT та LSFG для диференціації AQP4+ ON).
- Yang X et al. (2025). Advances in the treatment of neuromyelitis optic spectrum disorder. Therapeutic Advances in Neurological Disorders. PMC12033445 (огляд нових препаратів 2019–2024 рр. для AQP4+ NMOSD).
Для MOGAD та MOG-IgG
- Zara P et al. (2025). Applying the Supporting Features for MOGAD Diagnosis to Patients With Multiple Sclerosis. Neurology. PMC12509963 (застосування 2023 критеріїв MOGAD, supporting features для диференціації від MS).
- Stögbauer J et al. (2025). Therapeutic approaches in adults with myelin oligodendrocyte glycoprotein antibody-associated disease (MOGAD): A review of current evidence. Autoimmunity Reviews. DOI: 10.1016/j.autrev.2025.103231 (огляд гострого та профілактичного лікування MOGAD, стероїди, IVIG, ритуксимаб).
- 2023 International Diagnostic Criteria for MOGAD (Lancet Neurology, 2023, але активно цитується в 2024–2025) — ключовий для діагностики, з supporting MRI/clinical features.





