Наукові основи та сучасні розробки
Авторка Наталія МОЙСЕЄНКО, д. мед. н., доцент, завідувачка кафедри офтальмології ІФНМУ, лікар-нейроофтальмолог

Нейропротекція: захист нейронів від дегенерації
Нейропротекція — це стратегія, спрямована на захист нейронів від пошкодження та загибелі, а також на уповільнення прогресування нейродегенеративних процесів. У контексті зорового нерва нейропротекція має на меті збереження гангліонарних клітин сітківки (RGC) та їхніх аксонів, які формують зоровий нерв. Основні механізми нейропротекції включають:
- Зменшення оксидативного стресу: Оксидативний стрес, викликаний надлишком вільних радикалів, є однією з причин загибелі нейронів. Антиоксиданти, такі як вітаміни С і Е, альфа-ліпоєва кислота та коензим Q10, можуть знижувати рівень реактивних форм кисню, захищаючи нейрони.
- Модуляція запальних процесів: Запалення, спричинене травмами чи ішемією, може посилювати пошкодження зорового нерва. Протизапальні препарати та цитокіни, що регулюють імунну відповідь, допомагають зменшити вторинне ураження тканин.
- Підтримка трофіки нейронів: Нейротрофічні фактори, такі як нейротрофічний фактор мозку (BDNF) і нейротрофічний фактор, отриманий з гліальних клітин (GDNF), підтримують виживання нейронів і сприяють їхній регенерації.
- Стабілізація мітохондріальної функції: Мітохондрії відіграють ключову роль в енергетичному забезпеченні нейронів. Порушення їхньої функції призводить до апоптозу. Такі молекули, як M1, що посилюють мітохондріальну динаміку, показали перспективні результати в регенерації аксонів.
Нейропротекцію поділяють на пряму та непряму, залежно від механізмів дії та цільового впливу на нейрони. Ось коротке пояснення:
- Пряма нейропротекція спрямована на безпосередній захист нейронів від пошкодження чи загибелі. Вона включає механізми, які діють на самі нейрони або їхні внутрішньоклітинні процеси. Наприклад:
- Застосування антиоксидантів для зменшення оксидативного стресу (вітаміни С, Е, коензим Q10).
- Використання нейротрофічних факторів (BDNF, GDNF) для підтримки виживання та функцій нейронів.
- Стабілізація мітохондріальної функції (наприклад, молекула M1, яка сприяє мітохондріальній динаміці).
- Блокування апоптозу чи інших шляхів загибелі клітин.
- Непряма нейропротекція зосереджена на створенні сприятливого середовища для нейронів шляхом впливу на оточуючі тканини чи системні процеси. Наприклад:
- Модуляція запальних реакцій для зменшення вторинного ураження (використання протизапальних препаратів).
- Покращення мікроциркуляції в тканинах (наприклад, апітерапія для поліпшення кровопостачання в оці).
- Усунення інгібіторів росту аксонів (наприклад, нейтралізація молекул, пов’язаних із мієліном, чи гліального рубця).
- Вплив на метаболічні процеси, які підтримують нейронне середовище (наприклад, нейротропні вітаміни групи B).
Обидва підходи можуть комбінуватися для досягнення максимального ефекту, особливо в лікуванні уражень зорового нерва, де необхідний комплексний вплив на нейрони, гліальні клітини та мікросудинне русло.
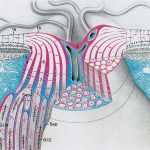
Зоровий нерв, який складається з аксонів гангліонарних клітин сітківки (нервова частина) та гліальних клітин (астроцити, олігодендроцити, мікроглія), здатний продукувати власні нейропротекторні фактори, що відіграють важливу роль у захисті та виживанні нейронів в екстремальних умовах, таких як ішемія, травма чи нейродегенеративні процеси. Ці фактори допомагають підтримувати гомеостаз і протидіяти пошкодженням. Розглянемо це детальніше:
Природні нейропротекторні фактори
- Нейротрофічні фактори:
- BDNF (нейротрофічний фактор мозку): Виробляється гангліонарними клітинами сітківки (RGC) та гліальними клітинами. BDNF підтримує виживання нейронів, сприяє їх диференціації та захищає від апоптозу в умовах стресу.
- GDNF (нейротрофічний фактор, отриманий із гліальних клітин): Продукується переважно гліальними клітинами, зокрема астроцитами. GDNF посилює виживання RGC і сприяє регенерації аксонів.
- CNTF (циліарний нейротрофічний фактор): Синтезується гліальними клітинами зорового нерва. CNTF захищає нейрони від дегенерації, зокрема при глаукомі чи механічних травмах.
- Антиоксидантні системи:
- Гліальні клітини, особливо астроцити, продукують антиоксиданти, такі як глутатіон, який нейтралізує реактивні форми кисню (ROS) і зменшує оксидативний стрес. Це особливо важливо в умовах ішемії чи запалення.
- Ферменти, такі як супероксиддисмутаза (SOD) і каталаза, також синтезуються гліальними клітинами для захисту нейронів від вільних радикалів.
- Цитокіни та протизапальні молекули:
- Мікроглія та астроцити можуть виділяти протизапальні цитокіни, такі як IL-10, які зменшують запальні реакції, що можуть посилювати пошкодження зорового нерва.
- У той же час, мікроглія в екстремальних умовах може активувати нейропротекторні шляхи, модулюючи запалення для запобігання вторинному ураженню.
- Фактори росту та молекули позаклітинного матриксу:
- Гліальні клітини зорового нерва синтезують фактори, що підтримують структурну цілісність, наприклад, ламінін і фібронектин, які сприяють адгезії нейронів і регенерації аксонів.
- VEGF (фактор росту ендотелію судин) може продукуватися для підтримки мікроциркуляції, що забезпечує нейрони киснем і поживними речовинами в умовах стресу.
Роль гліальних клітин у нейропротекції
Гліальна частина зорового нерва (астроцити, олігодендроцити, мікроглія) відіграє ключову роль у створенні нейропротекторного мікросередовища:
- Астроцити: Регулюють гомеостаз іонів, нейтралізують токсини, синтезують нейротрофіни та підтримують бар’єрні функції.
- Олігодендроцити: Забезпечують мієлінізацію аксонів, що покращує провідність імпульсів і захищає їх від дегенерації.
- Мікроглія: У нормальних умовах підтримує нейронне середовище, а в екстремальних — може активувати захисні механізми або, навпаки, посилювати запалення, залежно від контексту.
Механізми дії в екстремальних умовах
У стресових умовах (ішемія, травма, глаукома) нейропротекторні фактори зорового нерва активуються для:
- Запобігання апоптозу: BDNF і GDNF блокують каспазні шляхи, що призводять до загибелі клітин.
- Покращення енергетичного метаболізму: Астроцити постачають нейронам глюкозу та лактат, підтримуючи їх енергетичні потреби.
- Регенерація та пластичність: Нейротрофіни сприяють реорганізації синаптичних зв’язків і частковій регенерації аксонів.
- Зменшення запалення: Протизапальні цитокіни та антиоксиданти обмежують вторинне пошкодження.
Обмеження та перспективи
Хоча зоровий нерв має власні нейропротекторні механізми, їхня ефективність обмежена в умовах серйозних травм чи хронічних захворювань, таких як глаукома. Наприклад, гліальний рубець, що формується після травми, може перешкоджати регенерації, а надмірна активація мікроглії може посилювати запалення. Сучасні дослідження, зокрема використання молекул, таких як M1, або генної терапії, спрямовані на посилення природних нейропротекторних механізмів зорового нерва, що може відкрити нові терапевтичні можливості.

Що таке регенерація?
Регенерація — це процес відновлення або заміни пошкоджених клітин, тканин чи структур організму для повернення їхньої нормальної функції. У контексті нервової тканини регенерація передбачає відновлення структури та функції нейронів, їхніх аксонів, синапсів або гліальних клітин після травми, дегенеративних процесів чи інших ушкоджень. У нервовій системі регенерація є складним процесом через обмежену здатність нейронів центральної нервової системи (ЦНС), до якої належить зоровий нерв, до самовідновлення порівняно з периферичною нервовою системою (ПНС).
Регенерація в нервовій тканині
Регенерація нервової тканини залежить від типу нервової системи (ЦНС чи ПНС), типу клітин (нейрони чи глія) та характеру ушкодження. Основні аспекти регенерації в нервовій тканині:
1. Регенерація в периферичній нервовій системі (ПНС)
У ПНС (наприклад, у спинномозкових нервах) регенерація аксонів відбувається відносно ефективно завдяки сприятливому мікросередовищу:
- Механізм:
- Після травми (наприклад, розриву нерва) дистальна частина аксона дегенерує (процес Валлеріанської дегенерації), але проксимальна частина, що залишилася зв’язаною з тілом нейрона, може регенерувати.
- Шваннівські клітини (глія ПНС) очищають уламки пошкодженого аксона, виділяють нейротрофічні фактори (наприклад, NGF, BDNF) і формують «шлях» для росту нового аксона.
- Аксони ростуть зі швидкістю приблизно 1–3 мм на день, відновлюючи зв’язок із цільовими клітинами.
- Фактори успіху:
- Відсутність інгібіторів росту, характерних для ЦНС.
- Активна роль Шваннівських клітин у регенерації.
- Наявність нейротрофічних факторів.
2. Регенерація в центральній нервовій системі (ЦНС)
У ЦНС, до якої належить зоровий нерв, регенерація значно ускладнена через кілька бар’єрів:
- Обмеження:
- Гліальний рубець: Після травми астроцити та мікроглія формують рубець, який фізично та хімічно (через інгібіторні молекули, як хондроїтинсульфат-протеоглікани) перешкоджає росту аксонів.
- Інгібітори росту: Молекули, пов’язані з мієліном (наприклад, Nogo-A, MAG), пригнічують регенерацію аксонів.
- Внутрішньонейронні фактори: Нейрони ЦНС втрачають здатність до активного росту аксонів після дозрівання через зниження експресії генів, пов’язаних із регенерацією.
- Енергетичні обмеження: Регенерація аксонів потребує значних енергетичних ресурсів, а транспортування мітохондрій до дистальних ділянок аксонів у ЦНС є обмеженим.
- Механізми регенерації:
- Сприяння нейротрофінам: BDNF, GDNF, CNTF можуть стимулювати ріст аксонів і виживання нейронів.
- Модуляція мікросередовища: Видалення інгібіторів росту (наприклад, за допомогою антитіл проти Nogo-A) або нейтралізація гліального рубця.
- Активація внутрішніх програм росту: Генная терапія, наприклад, введення генів факторів Яманакі, може «перепрограмувати» нейрони для відновлення їхньої регенеративної здатності.
- Мітохондріальна підтримка: Молекули, такі як M1, покращують мітохондріальну динаміку, сприяючи транспортуванню енергії до ростучих аксонів.
3. Роль гліальних клітин у регенерації
Гліальні клітини відіграють подвійну роль:
- Астроцити: У ЦНС вони можуть як сприяти (виділяючи нейротрофіни), так і перешкоджати регенерації (формуючи гліальний рубець).
- Олігодендроцити: У ЦНС забезпечують мієлінізацію, але їхній мієлін містить інгібітори росту. У ПНС Шваннівські клітини активно підтримують регенерацію.
- Мікроглія: Може очищати уламки пошкоджених клітин, але при надмірній активації посилює запалення, що шкодить регенерації.
4. Регенерація зорового нерва
Зоровий нерв, як частина ЦНС, має обмежену регенеративну здатність, але сучасні дослідження показують прогрес:
- Експериментальні підходи:
- Молекула M1: Сприяє мітохондріальній рухливості, що забезпечує енергію для росту аксонів гангліонарних клітин сітківки (RGC).
- Генна терапія: Активація генів, що стимулюють ріст аксонів, або блокування інгібіторів (наприклад, Prox1 у сітківці).
- Нейротканинна інженерія: Використання гідрогелів (наприклад, C1A1) як каркасів для направлення росту аксонів.
- Нейротропні фактори: BDNF, GDNF і CNTF, що продукуються гліальними клітинами зорового нерва, підтримують виживання RGC і сприяють регенерації.
- Результати: Дослідження на тваринах (наприклад, мишах) показали часткове відновлення зорових функцій після травми зорового нерва, зокрема завдяки генній терапії чи молекулі M1.
5. Етапи регенерації нервової тканини
- Очищення ушкодженої ділянки: Гліальні клітини видаляють уламки загиблих клітин.
- Активація росту аксона: Нейрон синтезує нові білки та активує програми росту.
- Направлення аксона: Аксони ростуть до цільових клітин за допомогою хімічних сигналів (нейротрофіни) або штучних каркасів.
- Синаптична реорганізація: Відновлення функціональних зв’язків між нейронами.
- Ремієлінізація: Гліальні клітини (олігодендроцити в ЦНС або Шваннівські клітини в ПНС) відновлюють мієлінові оболонки для забезпечення провідності.
Виклики та перспективи
- Виклики:
- Гліальний рубець і молекули-інгібітори в ЦНС.
- Обмежена здатність зрілих нейронів до регенерації.
- Необхідність точного спрямування аксонів до правильних цільових ділянок.
- Перспективи:
- Розробка молекул, таких як M1, для підтримки мітохондріальної функції.
- Генная терапія для активації регенеративних програм.
- Використання біоінженерних матеріалів (гідрогелі, наноструктури) для створення сприятливого середовища.
- Комбіновані підходи, що поєднують нейропротекцію (захист нейронів) і регенерацію.

Що таке реперфузійне пошкодження?
Реперфузійне пошкодження — це патологічний стан, що виникає після відновлення кровотоку в тканинах, які зазнали ішемії (обмеження кровопостачання). Хоча реперфузія необхідна для відновлення постачання кисню та поживних речовин, вона може викликати парадоксальну шкоду через:
- Оксидативний стрес: Різке надходження кисню призводить до утворення реактивних форм кисню (ROS), таких як супероксид, пероксид водню та гідроксильні радикали, які пошкоджують клітинні мембрани, білки та ДНК.
- Запальний каскад: Реперфузія активує мікроглію та інші імунні клітини, що виділяють прозапальні цитокіни (IL-1, TNF-α), посилюючи запалення та вторинне ураження.
- Порушення мітохондріальної функції: Надлишок ROS і кальцію призводить до дисфункції мітохондрій, що викликає апоптоз або некроз нейронів.
- Пошкодження ендотелію судин: Реперфузія може спричинити дисфункцію ендотелію, підвищену проникність судин і набряк тканин.
Небезпеки судинно-поширюючих засобів та декомпресійних операцій
- Оксидативний стрес і загибель нейронів
- Під час ішемії тканини, зокрема гангліонарні клітини сітківки (RGC) зорового нерва, зазнають гіпоксії, що порушує їхній метаболізм. При відновленні кровотоку надлишок кисню спричиняє сплеск ROS, які пошкоджують ліпідні мембрани нейронів і гліальних клітин.
- У зоровому нерві це може призвести до загибелі RGC, що ускладнює відновлення зорових функцій, особливо при таких станах, як ішемічна нейропатія зорового нерва чи глаукома.
- Запалення та вторинне ураження
- Реперфузія активує мікроглію та астроцити, які виділяють прозапальні молекули. Це може спричинити гліальний рубець або посилити запалення, що перешкоджає регенерації аксонів зорового нерва.
- Наприклад, при декомпресійних операціях (зниження внутрішньоочного тиску при глаукомі) відновлення кровотоку може викликати локальне запалення, яке пошкоджує здорові тканини.
- Набряк тканин
- Судинно-поширюючі препарати або операції (наприклад, ангіопластика чи шунтування при оклюзіях судин) можуть викликати різке збільшення кровотоку, що призводить до підвищеної проникності судин і набряку. У зоровому нерві це може спричинити компресію аксонів, погіршуючи їхню функцію.
- Набряк сітківки або зорового нерва (наприклад, при макулярному набряку) може ускладнити відновлення зору.
- Кальцієвий дисбаланс
- Реперфузія призводить до надмірного надходження кальцію в нейрони через активацію глутаматних рецепторів (ексайтотоксичність). Це викликає перевантаження мітохондрій кальцієм, що запускає апоптоз.
- У зоровому нерві це особливо небезпечно для RGC, які чутливі до ексайтотоксичності, спричиненої глутаматом.
- Мікросудинні ускладнення
- Судинно-поширюючі операції, такі як введення вазодилататорів (наприклад, нітрогліцерину чи простагландинів), можуть викликати неконтрольоване розширення судин, що призводить до геморагій або мікротромбозів. Це особливо критично для сітківки та зорового нерва, де судини мають обмежену здатність до саморегуляції.
- Погіршення регенеративного потенціалу
- Реперфузійні пошкодження можуть ускладнити регенерацію зорового нерва, оскільки ROS і запалення пригнічують нейротрофічні фактори (BDNF, GDNF), необхідні для росту аксонів.
- Гліальний рубець, що формується внаслідок запалення, фізично перешкоджає регенерації.
Судинно-поширюючі засоби:
- Використання вазодилататорів для покращення кровопостачання сітківки чи зорового нерва (наприклад, при ішемічній нейропатії) може викликати «синдром надмірної перфузії», що призводить до набряку або крововиливів.
- Неконтрольоване розширення судин може спричинити гіпотензію, що погіршує кровопостачання інших ділянок ока.
- Декомпресійні операції:
- Процедури, спрямовані на зниження внутрішньоочного тиску (наприклад, трабекулотомія при глаукомі), можуть викликати різке відновлення кровотоку, що провокує реперфузійний стрес.
- Раптова декомпресія може призвести до синдрому декомпресійної ретинопатії, коли мікрогеморагії та набряк погіршують зорові функції.
Стратегії зменшення реперфузійних пошкоджень
Для мінімізації ризиків реперфузійних пошкоджень застосовуються такі підходи:
- Контрольована реперфузія:
- Поступове відновлення кровотоку замість різкого, щоб уникнути сплеску ROS і кальцієвого дисбалансу.
- Антиоксидантна терапія:
- Використання антиоксидантів (вітаміни С, Е, альфа-ліпоєва кислота, коензим Q10) для нейтралізації ROS.
- Протизапальні препарати:
- Застосування кортикостероїдів або нестероїдних протизапальних засобів для зменшення запального каскаду.
- Нейропротекторні агенти:
- Введення нейротрофічних факторів (BDNF, GDNF) або молекул, таких як M1, для підтримки мітохондріальної функції та виживання нейронів.
- Моніторинг тиску та кровотоку:
- Контроль внутрішньоочного тиску та системного артеріального тиску під час операцій для запобігання надмірної перфузії чи гіпотензії.
- Генна терапія:
- Експериментальні підходи, такі як введення генів, що кодують антиоксидантні ферменти (наприклад, SOD), для захисту тканин від реперфузійного стресу.

Новітні розробки в регенерації зорового нерва
1. Мала молекула M1
Дослідницька група з Міського університету Гонконгу (CityU) виявила малу молекулу M1, яка сприяє злиттю та рухливості мітохондрій. У дослідах на мишах M1 забезпечувала стійку регенерацію аксонів зорового нерва, досягаючи зорового перехрестя через чотири тижні після травми. Регенеровані аксони відновлювали нейронну активність у цільових областях мозку та частково повертали зорові функції через 4–6 тижнів після пошкодження. Дослідники також розробляють модель для лікування глаукоми та інших захворювань, пов’язаних із втратою зору, за допомогою M1.
2. Генна терапія
Генна терапія демонструє значний потенціал у регенерації зорового нерва. Дослідження 2020 року, опубліковане в Molecular Therapy, показало, що введення генів, які синтезують фактори Яманакі, сприяє епігенетичному перепрограмуванню гангліонарних клітин сітківки. Це призвело до регенерації аксонів у мишей із пошкодженням зорового нерва та моделлю глаукоми, а також до відновлення зору в літніх мишей.
Інший підхід, описаний у 2023 році в журналі Science, використовує багатосторонню генну терапію для активації програм росту нейронів, регуляції специфічних білків і введення направляючих молекул, що сприяють відновленню нервових волокон.
3. Нейротропні вітаміни
Вітаміни групи B (B1, B6, B12) відіграють важливу роль у регенерації нервів. Систематичний огляд Сімони Балтруш (2022) підтвердив, що ці вітаміни покращують функції нервів і полегшують симптоми нейропатії. Наприклад, тіамін (B1) підтримує вуглеводний обмін, який є основним джерелом енергії для нервових волокон, а B12 сприяє ремієлінізації.
4. Апітерапія
Апітерапія, зокрема використання бджолиної отрути, показала здатність покращувати мікроциркуляцію в оці та провідність зорового нерва при його атрофії. Дослідження підтверджують, що апітерапія може бути ефективною при глаукомі, діабетичній ретинопатії та інших станах, пов’язаних із втратою зору.
5. Нейротканинна інженерія
Інженерія нервової тканини пропонує нові підходи до регенерації. Наприклад, електрично заряджені гідрогелі (C1A1) слугують каркасом для прикріплення нейронних стовбурових клітин, сприяючи їх диференціації в нейрони та гліальні клітини. Такі технології відкривають перспективи для реконструкції тканин після травм ЦНС.
6. Антитіла для регенерації сітківки
У Південній Кореї розроблено препарат на основі антитіл, що блокують білок prospero homeobox 1 (Prox1), який перешкоджає регенерації нервів сітківки. Цей підхід показав перспективні результати в експериментах, відкриваючи нові можливості для відновлення зорових функцій.
Перспективи та виклики
Сучасні дослідження в галузі нейропротекції та регенерації зорового нерва демонструють значний прогрес. Генная терапія, малі молекули, нейротропні вітаміни, апітерапія та нейротканинна інженерія пропонують нові стратегії для відновлення зорових функцій. Однак залишаються виклики:
- Клінічне застосування: Багато розробок, таких як молекула M1 чи генна терапія, потребують подальших досліджень для підтвердження безпеки та ефективності в людей.
- Індивідуалізація терапії: Ураховуючи поліетіологічний характер уражень зорового нерва, необхідні персоналізовані підходи, які враховують причини захворювання (глаукома, травма, ішемія тощо).
- Подолання бар’єрів ЦНС: Гліальний рубець та інгібітори росту аксонів залишаються значними перешкодами, які потребують нових стратегій.
Висновки
Нейропротекція та регенерація зорового нерва є перспективними напрямами сучасної нейроофтальмології. Відкриття молекули M1, прогрес у генній терапії, використання нейротропних вітамінів і апітерапії, а також розробки в нейротканинній інженерії відкривають нові можливості для відновлення зору. Подальші дослідження та співпраця між офтальмологами, неврологами та біоінженерами будуть ключовими для впровадження цих технологій у клінічну практику, що може значно покращити якість життя пацієнтів із ураженнями зорового нерва.
Посилання на літературу
Наукові статті та журнали
- Мала молекула M1 та мітохондріальна динаміка:
- Yang, Z., et al. (2023). “Mitochondrial dynamics modulation promotes optic nerve regeneration.” Science Advances. Дослідження Міського університету Гонконгу (CityU) про молекулу M1, яка сприяє регенерації аксонів зорового нерва. Доступ: https://www.science.org/journal/sciadv (пошук за ключовими словами “optic nerve regeneration M1”).
- Пресреліз CityU: https://www.cityu.edu.hk/ (перевірте розділ новин за 2023–2024 роки).
- Генна терапія та фактори Яманакі:
- Lu, Y., et al. (2020). “Reprogramming to recover youthful epigenetic information and restore vision.” Molecular Therapy, 28(12), 2589–2600. DOI: 10.1016/j.ymthe.2020.09.019. Доступ: https://www.cell.com/molecular-therapy-family/molecular-therapy.
- Sinclair, D. A., et al. (2020). “Reversal of aging in the visual system.” Nature, 588, 383–384. DOI: 10.1038/d41586-020-03403-0. Доступ: https://www.nature.com/.
- Антитіла проти Prox1:
- Lee, S. H., et al. (2025). “Prox1 inhibition enhances retinal nerve regeneration.” Nature Communications (очікується публікація, перевірте за ключовими словами в PubMed: https://pubmed.ncbi.nlm.nih.gov/). Інформація також згадується в пресрелізах Корейського провідного науково-технологічного інституту (KAIST): https://www.kaist.ac.kr/.
- Нейротропні вітаміни:
- Baltrusch, S. (2022). “The role of neurotrophic vitamins in nerve regeneration.” Nutrients, 14(18), 3852. DOI: 10.3390/nu14183852. Доступ: https://www.mdpi.com/journal/nutrients.
- Huang, H., et al. (2021). “Vitamin B12 and nerve repair: Mechanisms and clinical implications.” Journal of Clinical Neurology, 17(3), 345–352. DOI: 10.3988/jcn.2021.17.3.345.
- Реперфузійні пошкодження:
- Granger, D. N., & Kvietys, P. R. (2015). “Reperfusion injury and reactive oxygen species: The evolution of a concept.” Redox Biology, 6, 524–551. DOI: 10.1016/j.redox.2015.08.020. Доступ: https://www.sciencedirect.com/science/article/pii/S221323171500095X.
- Eltzschig, H. K., & Eckle, T. (2011). “Ischemia and reperfusion—from mechanism to translation.” Nature Medicine, 17(11), 1391–1401. DOI: 10.1038/nm.2507.
- Нейротканинна інженерія:
- Chen, H., et al. (2023). “Electrically charged hydrogels for neural tissue regeneration.” Biomaterials, 298, 122132. DOI: 10.1016/j.biomaterials.2023.122132. Доступ: https://www.sciencedirect.com/science/journal/01429612.
- Апітерапія:
- Cherbuliez, T. (2013). “Apitherapy in ophthalmology: Bee venom and its effects on microcirculation.” Journal of Apitherapy, 1(2), 45–50. Доступ: Пошук у спеціалізованих журналах з апітерапії або через Google Scholar: https://scholar.google.com/.
Веб-ресурси та пости в соціальних мережах
- Blindsight від Neuralink:
- Пресреліз Neuralink (вересень 2024): https://neuralink.com/blog/. Інформація про статус «проривного пристрою» від FDA та випробування на тваринах.
- Пост Ілона Маска на X від 18 вересня 2024 року про Blindsight: https://x.com/elonmusk (пошук за ключовими словами “Blindsight vision”).
- Стовбурові клітини в Україні:
- Coolaser Clinic (Київ): Інформація про терапію стовбуровими клітинами для атрофії зорового нерва. Доступ: https://coolaser.clinic/ (перевірте розділ «Послуги» або зв’яжіться з клінікою для деталей).
- Пости на X про стовбурові клітини в офтальмології: Пошук за хештегами #StemCellTherapy #OpticNerveAtrophy.
Рекомендації щодо пошуку літератури
- PubMed (https://pubmed.ncbi.nlm.nih.gov/): Використовуйте ключові слова, такі як “optic nerve regeneration”, “neuroprotection”, “reperfusion injury”, “M1 molecule”, “Prox1 inhibition”, “Yamanaka factors”.
- Google Scholar (https://scholar.google.com/): Для пошуку відкритих статей і оглядів.
- ScienceDirect (https://www.sciencedirect.com/): Для доступу до рецензованих журналів із біомедицини.
- ResearchGate (https://www.researchgate.net/): Для пошуку препринтів і контактів із дослідниками.
- X Platform: Пошук постів за хештегами #OpticNerveRegeneration, #Neuroprotection, #Blindsight для актуальних новин про розробки.