Загадкові клітини: клітини Мюллера, астроцити та олігодендроцити — що ми про них знаємо сьогодні?
Авторка Наталія МОЙСЕЄНКО, д. мед. н., доцент, завідувачка кафедри офтальмології ІФНМУ, лікар-нейроофтальмолог
Друзі, як часто ви чуєте від пацієнтів: «Я роками відчуваю, що з зором щось не так — розмитість, втрата яскравості кольорів, звуження полів зору, — а лікарі кажуть, що все нормально»? Роками ходять по колу, роблять стандартні перевірки, але справжньої причини не знаходять. Це не ваша вина. В Україні офтальмологи в поліклініках часто не знають, коли саме потрібно направляти до нейроофтальмолога — така практика не поширена, протоколи недосконалі. В результаті люди втрачають шанс на відновлення або суттєве покращення зору там, де це ще можливо. Час — це зір, і його не повернути назад.
Сьогодні хочу розповісти про «загадкових» учасників цих подій — гліальні клітини зорового нерва та сітківки: клітини Мюллера, астроцити та олігодендроцити. Довгий час ми фокусувалися тільки на гангліозних клітинах сітківки та їх аксонах, але сучасні дослідження показують: саме глія — це «сцена», на якій розгортається вся драма оптичних невропатій (глаукома, ішемічні, запальні, демієлінізуючі процеси, спадкові атрофії тощо). Вони не просто підтримують нейрони — вони активно визначають, чи виживуть аксони, чи загинуть.
Клітини Мюллера
Клітини Мюллера — це радіальні глії сітківки, єдині клітини, що пронизують усю товщу сітківки від зовнішньої до внутрішньої обмежувальної мембрани. У нормі вони:
- підтримують структуру сітківки,
- регулюють іонний баланс (особливо калій),
- забирають надлишок глутамату (щоб уникнути ексайтотоксичності), живлять нейрони, транспортують глюкозу та метаболіти.
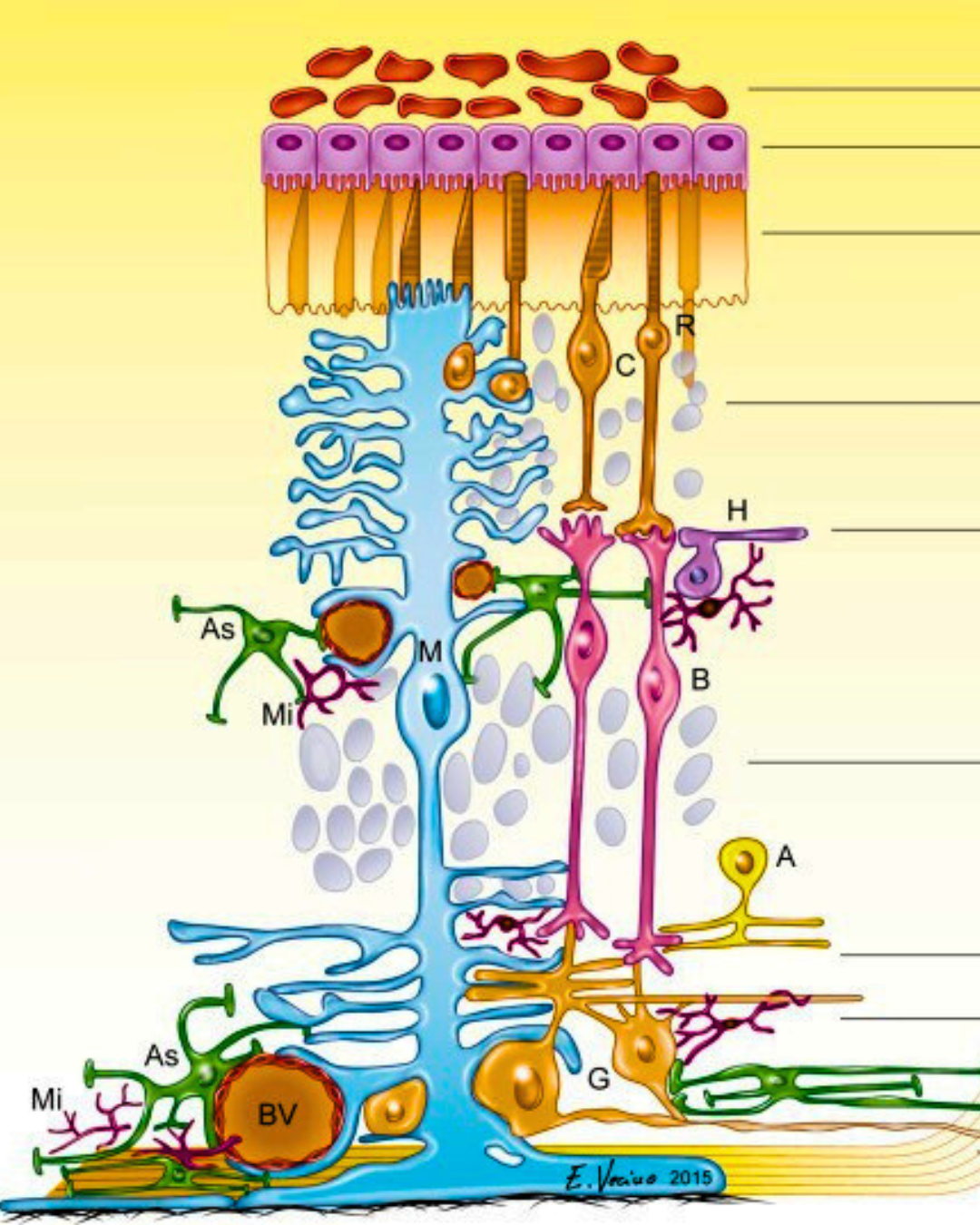
Астроцити
Астроцити — головні «охоронці» в ділянці lamina cribrosa (optic nerve head) та самого зорового нерва. Вони:
- регулюють кровотік,
- підтримують енергетичний баланс,
- формують бар’єр,
- контролюють вузли Ранв’є.
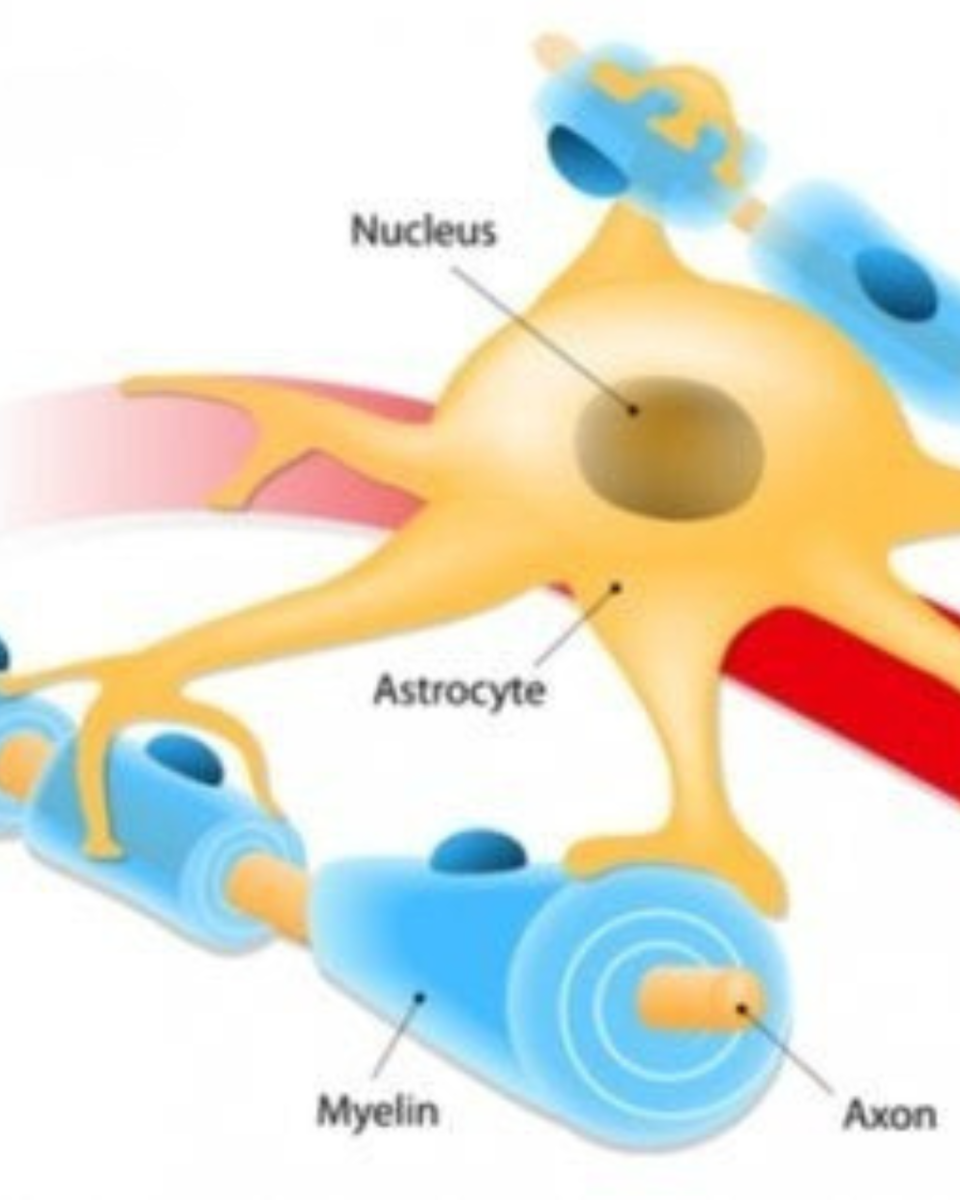
Олігодендроцити
Олігодендроцити — створюють мієлін у зоровому нерві (поза сітківкою, починаючи від lamina cribrosa). Без якісного мієліну імпульс передається повільно, аксони стають вразливими до енергетичного дефіциту. У демієлінізуючих невропатіях (NMOSD, MOG-асоційовані, розсіяний склероз, Leber’s hereditary optic neuropathy) олігодендроцити страждають першими: втрата мієліну → блокада провідності → аксональна дегенерація. Цікаво, що в глаукомі теж виявляють демієлінізацію та втрату олігодендроцитів — іноді ще до вираженої втрати гангліозних клітин. Це робить зоровий нерв особливо чутливим до метаболічних порушень.
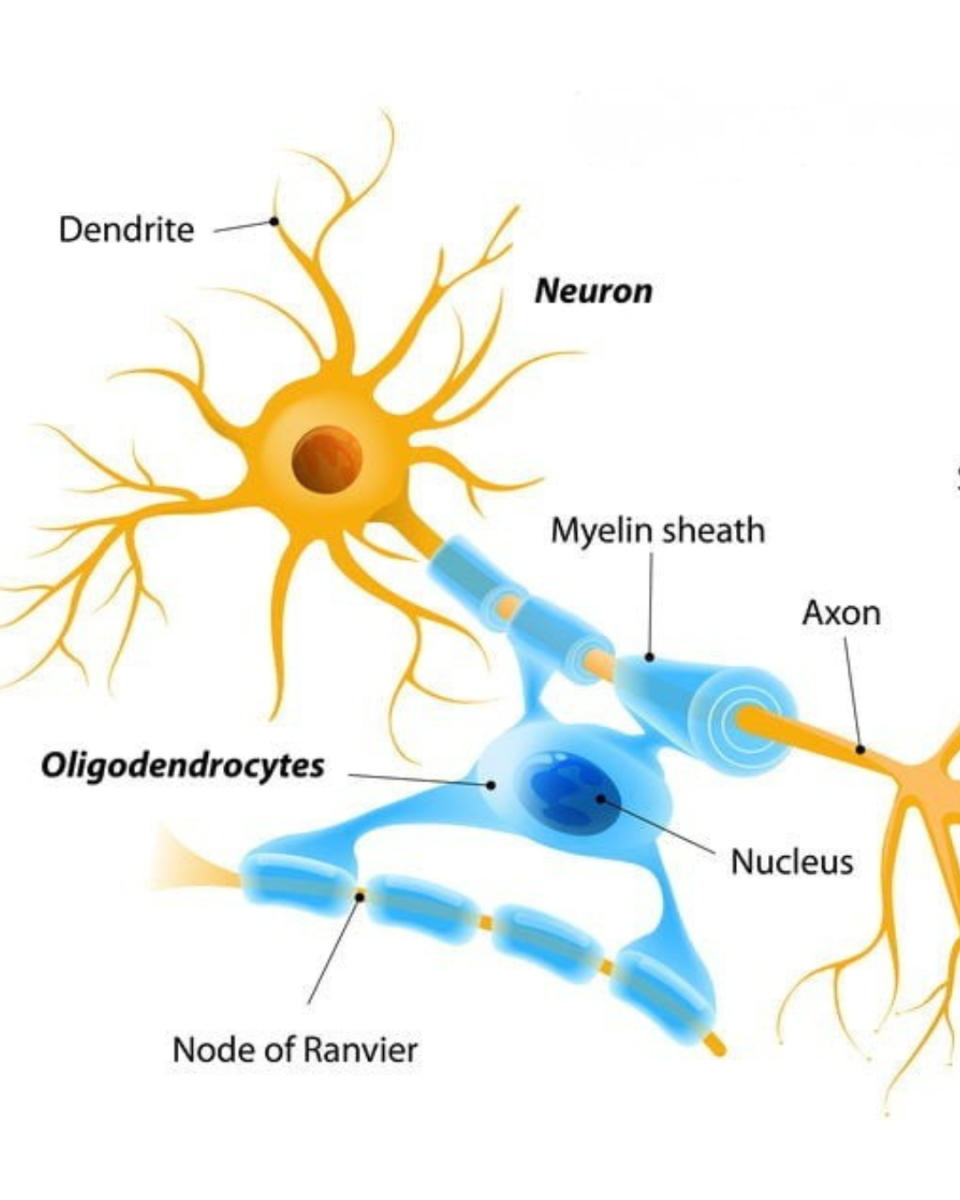
Відмінності: де вони живуть і чому це принципово
Клітини Мюллера — унікальна радіальна глія, яка існує виключно в сітківці (внутрішньоочна частина зорового шляху). Вони пронизують усю товщу сітківки від зовнішньої до внутрішньої обмежувальної мембрани, як опорні стовпи. Це «ретинальна» глія, яка ніколи не виходить за межі сітківки. Астроцити та олігодендроцити — це «мозкові» гліальні клітини, які працюють у зоровому нерві поза сітківкою (починаючи від lamina cribrosa — решітчастої пластинки — і далі до мозку). Астроцити розташовані в optic nerve head, myelinated optic nerve та частково в nerve fiber layer сітківки, а олігодендроцити — тільки в мієлінізованій частині зорового нерва (поза lamina cribrosa).
Ця локалізація визначає їхню спеціалізацію: клітини Мюллера «працюють» з сітківковими нейронами та гангліозними клітинами безпосередньо в сітківці, тоді як астроцити та олігодендроцити захищають і підтримують аксони вже в зоровому нерві. У патології (глаукома, ішемія, запалення) порушення в одній зоні швидко впливає на іншу — тому комплексне обстеження обов’язкове.
Спільні риси: чому вони — справжні «охоронці» зору
Незважаючи на відмінності в розташуванні, ці клітини мають багато спільного — і саме це робить їх ключовими в оптичних невропатіях:
- Живлення та метаболічна підтримка — забезпечують нейрони глюкозою, метаболітами, допомагають у енергетичному балансі (особливо важливе для аксонів з високим енергоспоживанням).
- Бар’єрна функція — формують гемато-ретинальний і гемато-енцефалічний бар’єри, регулюють проникність судин, захищають від токсинів. Ізоляція та провідність — олігодендроцити створюють мієлін для швидкої передачі імпульсів; астроцити та клітини Мюллера контролюють вузли Ранв’є та іонний баланс (особливо калій).
- Регуляція нейротрансмітерів — забирають надлишок глутамату (щоб уникнути ексайтотоксичності), модулюють синаптичну активність.
- Виживання нейронів у критичних ситуаціях — у стресі (ішемія, запалення, травма) вони виділяють нейротрофічні фактори (BDNF, GDNF, NGF, CNTF), намагаючись врятувати аксони та гангліозні клітини.
- Роль у цитоскелеті та потенційній регенерації — у реактивному стані формують щільний цитоскелет (гліоз), який може стати «каркасом» для майбутньої регенерації аксонів (хоча часто це призводить до рубцювання та стиснення).
У нормі — союзники. У патології — можуть стати «двосічним мечем»: реактивний гліоз іноді захищає, іноді прискорює загибель (виділяють запальні цитокіни, стискають аксони, порушують транспорт мітохондрій).
При невриті зорового нерва (optic neuritis, часто демієлінізуючий)
Це гострий запальний процес, де імунна атака спрямована на мієлін (розсіяний склероз, NMOSD, MOG-асоційовані тощо). Олігодендроцити страждають першими: втрата мієліну блокує провідність, призводить до аксональної дегенерації. Астроцити реагують реактивним гліозом: намагаються обмежити запалення, виділяють нейротрофіни для захисту аксонів, але в хронічній фазі утворюють рубцеву тканину, яка блокує ремієлінізацію. Клітини Мюллера в сітківці активуються: регулюють глутамат (щоб уникнути ексайтотоксичності), виділяють фактори росту, але при сильному запаленні сприяють апоптозу гангліозних клітин. Реактивна глія тут — «двосічний меч»: ранній захист, але пізніше — перешкода для відновлення.
Чому глія — ключова мішень при невриті?
Неврит зорового нерва — це не просто запалення аксонів гангліозних клітин сітківки. У аутоімунних формах (як NMOSD, MOGAD, серонегативні випадки) імунна атака первинно спрямована на гліальні клітини або їхні поверхневі антигени:
- Астроцити (мозкові глії, особливо в optic nerve head та lamina cribrosa) — головна мішень при AQP4-IgG-позитивному NMOSD. Антитіла до аквапорину-4 (AQP4) зв’язуються з AQP4 на ендфут астроцитів, активують комплемент, викликають цитотоксичність (CDC та ADCC), призводять до лізису астроцитів, порушення бар’єру, набряку та вторинної демієлінізації. Астроцити втрачають AQP4 та GFAP, формується астроклітинна патологія — це відрізняє NMOSD від MS. Реактивні астроцити намагаються захищати (виділяють нейротрофіни), але часто стають джерелом запалення та рубцювання.
- Олігодендроцити (створюють мієлін у зоровому нерві поза lamina cribrosa) — первинна мішень при MOG-IgG-позитивному MOGAD. Антитіла до мієлінового олігодендроцитарного глікопротеїну (MOG) зв’язуються з MOG на поверхні олігодендроцитів та зовнішньому шарі мієліну, викликають ADCC, активацію комплементу, пряме пошкодження олігодендроцитів, демієлінізацію без значного ураження астроцитів. Це пояснює кращий прогноз відновлення при MOGAD порівняно з NMOSD — астроцити зберігаються, ремієлінізація можлива. Патологія: добре окреслені зони демієлінізації, відносне збереження аксонів та астроцитів, інфільтрація гранулоцитами та макрофагами.
- Клітини Мюллера (ретинальна глія) — вторинно залучаються в усіх формах, особливо при сильному запаленні чи ішемії. Вони реагують реактивно: регулюють глутамат (щоб уникнути токсичності), виділяють BDNF/GDNF для захисту гангліозних клітин, але при аутоімунній атаці можуть посилювати запалення (цитокіни TNF-α, IL-1β), сприяти апоптозу. У NMOSD (AQP4+) клітини Мюллера теж експресують AQP4, тому можуть бути безпосередньо уражені.
У всіх випадках імунні комплекси (антитіла + комплемент) осідають периваскулярно, активують мікроглію, залучають гранулоцити/макрофаги, призводять до набряку, демієлінізації та аксональної дегенерації. Глія — не просто «підтримка», а первинна мішень, на яку виробляються антитіла, провокуючи весь процес.
НАІОН або передня ішемічна невропатія
НАІОН (неартеритичній передній ішемічній оптичній невропатії) — одній з найпоширеніших причин гострої втрати зору після 50 років — люди втрачають шанс на обмеження пошкодження та збереження зору там, де це ще можливо. Час — це зір, і його не повернути.
Сьогодні фокус на НАІОН і ключовій ролі клітин Мюллера — ретинальної глії, яка перша реагує на ішемію через порушення кровопостачання дрібних судин (коротких задніх циліарних артерій). Саме вони стають «першою лінією оборони» та створюють бар’єр для подальшого пошкодження, хоча іноді це може мати й негативні наслідки.
Чому клітини Мюллера грають більшу роль при НАІОН?
НАІОН — це ішемія головки зорового нерва (optic nerve head), часто в «тісному» диску (crowded disc), де виникає набряк, компартмент-синдром: набряклі аксони стискаються в обмеженому просторі lamina cribrosa, це призводить до апоптозу гангліозних клітин сітківки (RGC) та їх аксонів. Запалення мінімальне, але ішемія запускає каскад.
Клітини Мюллера (внутрішньоочна глія, пронизують усю сітківку) реагують першими, бо вони безпосередньо контактують з гангліозними клітинами та їх аксонами в сітківці (nerve fiber layer та ganglion cell layer). При ішемії:
- Вони швидко активуються: змінюють метаболізм, перерозподіляють іони (калій, натрій), забирають надлишок глутамату (щоб уникнути ексайтотоксичності — перезбудження нейронів).
- Виділяють нейротрофічні фактори (BDNF, GDNF, NGF), намагаючись підтримати виживання RGC.
- Формують реактивний гліоз: розростаються, утворюють щільний бар’єр (як scar-подібну структуру), який обмежує поширення ішемії та набряку вглиб сітківки, захищає від подальшого пошкодження сусідніх нейронів.
- У моделях rAION (rodent NAION) та ішемії-реperfusion показано, що реактивні клітини Мюллера беруть участь у ранній відповіді на дистрес RGC, підтримують їх метаболічно та структурно.
Це створює захисний бар’єр — вони намагаються локалізувати пошкодження, регулюють іонний баланс та запобігають масовій ексайтотоксичності.
Подальше залучення астроцитів (мозкові глії в optic nerve head та lamina cribrosa) відбувається пізніше: вони теж реагують реактивним гліозом, проліферують, намагаються заповнити «порожнечу» від загиблих аксонів, виділяють нейротрофіни. Але при сильній ішемії це призводить до порушення балансу нейротрансмітерів (глутамат накопичується, викликає перезбудження), стиснення аксонів рубцевою тканиною, порушення транспорту мітохондрій та енергетичного дефіциту — що посилює загибель.
Олігодендроцити менш задіяні гостро (ішемія в передній немієлінізованій частині), але пізніше втрата мієліну прискорює дегенерацію.
Клітини Мюллера — перші реагенти на ішемію в сітківці, створюють бар’єр, намагаються врятувати RGC. Але якщо процес не зупинити, реактивна глія може перейти в деструктивну фазу.
Саме тому при підозрі на НАІОН (раптова втрата, набряк диска без запалення) не можна чекати. Потрібен повний пакет обстежень за один візит: ОКТ (RNFL + шар гангліозних клітин), поля зору (Humphrey/Octopus, альтитудинальний дефект), кольоровий тест, електрофізіологія (ПЗВП), іноді флюоресцентна ангіографія чи МРТ (щоб виключити інші причини). Це зручно, швидко та дає повну картину.
Чому рання вазодилатація небезпечна при НАІОН?
Рання судиннорозширювальна терапія (наприклад, PGE1, інші вазодилататори) намагається швидко відновити кровотік — здається логічним. Але в умовах компартмент-синдрому та набряку це часто призводить до реперфузійних пошкоджень (ischemia-reperfusion injury):
Сучасні дані (2023–2025 рр.) показують: немає доказової користі від ранніх вазодилататорів при НАІОН, а ризики реперфузійного пошкодження високі. Багато досліджень фокусуються на контролі факторів ризику (гіпертензія, апное, гіперліпідемія), а не на агресивній вазодилатації.
Роль загадкових клітин при глаукомі:
Сьогодні розберемо, як саме гліальні клітини — астроцити та клітини Мюллера — відіграють ключову роль при глаукомі. Вони не просто підтримують структуру — вони є елементами заднього шляху відтоку внутрішньоочної рідини та глімфатичної системи ока (ocular glymphatic system), яка очищає сітківку та зоровий нерв від метаболічних відходів, токсинів (включаючи β-амілоїд) та надлишкової рідини. Дисфункція цих клітин сприяє накопиченню відходів, посилює нейродегенерацію гангліозних клітин сітківки (RGC) та прогресію глаукоми, навіть при контрольованому внутрішньоочному тиску (ВОТ).
Глімфатична система ока та задній шлях відтоку: що це?
Глімфатична система — це периваскулярна мережа, залежна від гліальних клітин (аналогічна мозковій глімфатичній системі), яка забезпечує очищення інтерстиціальної рідини та метаболічних відходів з сітківки та зорового нерва. У глаукомі порушення цієї системи призводить до накопичення токсинів, запалення та загибелі RGC. Задній шлях відтоку включає:
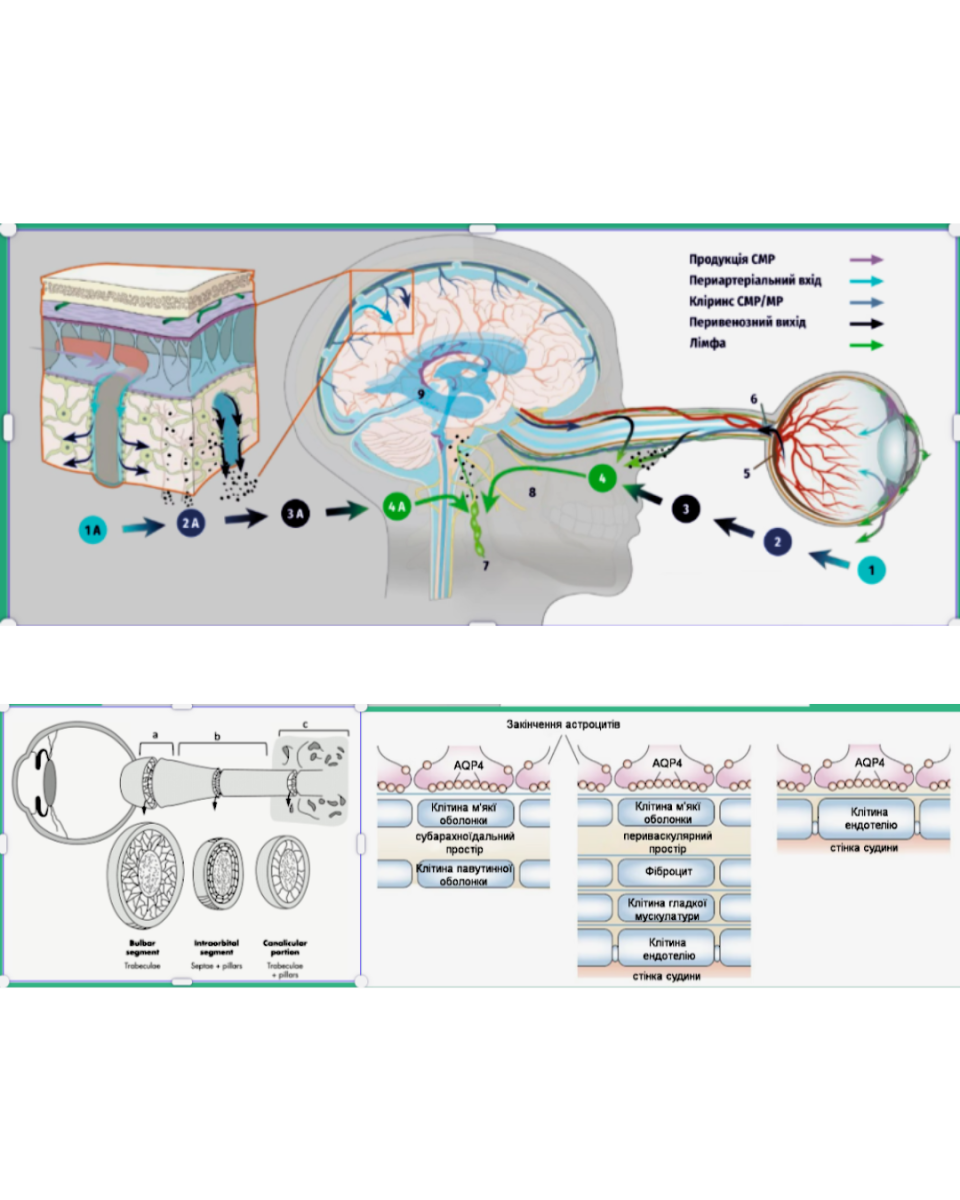
- Клітини Мюллера (ретинальна глія) — пронизують усю сітківку, експресують AQP4 (аквапорин-4) для транспорту води. Вони очищають воду з внутрішньої сітківки, направляють її до склистого тіла, ретинальних судин та субретинального простору. При глаукомі дисфункція Мюллерівських клітин порушує цей транспорт, призводить до набряку сітківки, накопичення відходів та ексайтотоксичності (надлишок глутамату).
- Астроцити (головні в optic nerve head та lamina cribrosa) — формують периваскулярні простори, регулюють потік рідини вздовж зорового нерва до субарахноїдального простору та шийних лімфатичних вузлів. Вони експресують AQP4 на ендфут, забезпечують очищення CSF-подібної рідини. При глаукомі реактивні астроцити перебудовують позаклітинний матрикс, стискають аксони в lamina cribrosa, порушують транспорт мітохондрій та енергетику, сприяють рубцюванню та блокаді глімфатичного потоку.
Дисфункція цих клітин (реактивний гліоз, втрата AQP4, запальні цитокіни) призводить до:
- Накопичення токсинів (β-амілоїд, тау тощо) в сітківці та зоровому нерві.
- Порушення очищення інтерстиціальної рідини → хронічний стрес RGC.
- Посилення нейродегенерації, навіть при нормальному ВОТ (нормальний тиск глаукома).
- Збільшення периваскулярних просторів або, навпаки, їх блокада — патологічні зміни глімфатичного потоку.
У моделях глаукоми показано, що дисфункція глії починається рано — ще до вираженої втрати RGC, роблячи астроцити та клітини Мюллера ключовими гравцями в патогенезі.
Саме тому при підозрі на глаукому (підвищений ВОТ, дефекти полів, зміни на ОКТ) не можна обмежуватися «очним дном» чи тонометрією. Потрібен повний пакет обстежень за один візит: ОКТ (RNFL + шар гангліозних клітин), поля зору (Humphrey/Octopus), кольоровий тест, електрофізіологія (ПЗВП, мультифокальна ЕРГ), іноді МРТ чи додаткові аналізи. Це зручно, швидко та дає повну картину — без втрати часу.
- раптове зниження зору на одне око (часто за 1–3 дні)
- біль за оком або в оці, що посилюється при русі очима
- порушення кольоросприйняття (особливо червоний колір виглядає тьмяним або сірим)
- відносний аферентний дефект зіниці (RAPD) при світловій реакції
- набряк диска зорового нерва на офтальмоскопії (але важливо: у 30–40% випадків диска може не бути набряку — це ретробульбарний неврит, і тоді очне дно виглядає нормальним)
Висновок
Друзі, ми пройшли довгий шлях через ці статті: від загадкових клітин Мюллера, астроцитів та олігодендроцитів — до їхньої ролі при невриті зорового нерва, НАІОН та глаукомі. Ми побачили, що ці «невидимі охоронці» не просто підтримують нейрони — вони визначають, чи вдасться обмежити пошкодження, чи процес піде далі. Вони першими реагують на ішемію, запалення чи хронічний тиск, намагаються створити бар’єр, очистити тканини, врятувати аксони — але іноді стають частиною проблеми: реактивний гліоз, порушення глімфатичного очищення, дисбаланс нейротрансмітерів, рубцювання.
Головне, що ми зрозуміли: більшість оптичних невропатій — це не тільки справа самих гангліозних клітин і аксонів. Це комплексна взаємодія з глією, і саме тому стандартні перевірки в поліклініці часто не дають відповіді. Люди роками живуть із розмитістю, втратою полів зору, тьмяними кольорами, раптовими «завісами» — і не отримують адекватного лікування. Це не ваша вина. В Україні практика направлення до нейроофтальмолога не поширена, протоколи недосконалі, і в результаті шанс на відновлення або суттєве уповільнення прогресії втрачається там, де він ще є.
Саме тому я постійно наголошую: не чекайте. Якщо ви відчуваєте, що «щось не так із зором» — пишіть або записуйтесь негайно. Перша консультація — це завжди лише знайомство, збір анамнезу та складання індивідуального плану. Але далі ми організовуємо все максимально швидко: повний пакет обстежень за один візит — ОКТ (шар гангліозних клітин + RNFL), поля зору, кольоровий тест, електрофізіологія (ПЗВП, мультифокальна ЕРГ), МРТ з контрастом, специфічні аналізи (AQP4, MOG тощо, якщо підозра на аутоімунний процес). Це зручно, швидко та дає повну картину без втрати часу.
Щодо високодозової (пульс-терапії) кортикостероїдами — так, вона викликає страх: побічні ефекти, ускладнення, довгий список протипоказів. Багато пацієнтів чули страшні історії або читають в інтернеті, що «це небезпечно». Але в гострих запальних невритах (особливо AQP4+ NMOSD), при деяких формах з набряком диска, саме пульс-терапія часто повертає зір, коли низькі дози, пероральні препарати чи альтернативні методи вже не діють. У НАІОН та глаукомі її застосовують рідко або взагалі не застосовують — там пріоритет на контролі факторів ризику, нейропротекції, лазері чи хірургії. Рішення завжди індивідуальне, зважуючи докази, ризики та користь — і тільки після повного обстеження.
Висновок простий: сучасна нейроофтальмологія вже не обмежується «очним дном» і тиском. Ми розуміємо, що глія — це ключ до розуміння, чому в одних пацієнтів зір падає швидко, в інших — стабільно, чому деякі відновлюються добре, а інші втрачають усе. І саме тому рання, точна діагностика та індивідуальний підхід дають реальний шанс зберегти або повернути зір.
Якщо ви або ваші близькі вже довго живете з цими симптомами — не відкладайте. Напишіть мені зараз. Разом ми розберемося, що відбувається з цими загадковими клітинами у вашому випадку і що можна зробити, щоб не втратити більше.
Бережіть зір. Він безцінний ❤️ Наталія Мойсеєнко
Рекомендовані джерела літератури
Рекомендована література з нейроофтальмології: ключові джерела для розуміння ролі глії в оптичних невропатіях
Друзі, багато хто з вас роками живе з порушеннями зору — розмитістю, втратою полів зору, тьмяними кольорами, раптовими «завісами» чи поступовим звуженням — і не може знайти пояснення чи ефективне лікування. Це не ваша вина. В Україні офтальмологи в поліклініках часто не знають, коли саме потрібно направляти до нейроофтальмолога — така практика не поширена, протоколи недосконалі. В результаті люди втрачають шанс на відновлення або суттєве уповільнення прогресії там, де це ще можливо. Час — це зір, і його не повернути.
Сьогодні хочу дати вам список рекомендованої літератури — це ключові огляди, статті та книги, які допомагають зрозуміти роль гліальних клітин (Мюллера, астроцитів, олігодендроцитів) у патогенезі невриту зорового нерва, НАІОН та глаукоми. Ці джерела — основа сучасної доказової нейроофтальмології.
Ключові огляди та статті (2020–2025 роки)
- Glial Cells in Glaucoma: Friends or Foes? Автор: Calkins DJ, Horner PJ et al. Журнал: Progress in Retinal and Eye Research, 2023 Ключові слова: reactive astrogliosis, Müller glia, lamina cribrosa remodeling, glymphatic dysfunction in glaucoma.
- Astrocyte Reactivity in Optic Nerve Head in Glaucoma and NAION Автор: Sun D, Qu J, Jakobs TC. Журнал: Investigative Ophthalmology & Visual Science, 2022–2024 серія статей Фокус: астроцити в lamina cribrosa, компартмент-синдром, реперфузійні пошкодження.
- Müller Glia in Retinal Ischemia and NAION Models Автор: Bringmann A, Wiedemann P. Журнал: Cells, 2023 Детально про першу реакцію клітин Мюллера на ішемію, захисний бар’єр та ексайтотоксичність.
- AQP4-IgG and MOG-IgG Associated Optic Neuritis: Glial Targets Автор: Chen JJ, Pittock SJ, Flanagan EP et al. Журнал: Lancet Neurology, 2021–2024 (огляди та consensus) Класика для розуміння, чому астроцити та олігодендроцити — первинні мішені при NMOSD та MOGAD.
- The Ocular Glymphatic System: Implications for Glaucoma and Neurodegeneration Автор: Mathieu E, Gupta N, Ahari A, Yücel YH. Журнал: Frontiers in Neuroscience, 2022–2025 Про глімфатичну систему ока, роль AQP4 на астроцитах та клітинах Мюллера, порушення очищення при глаукомі.
- Ischemia-Reperfusion Injury in Non-Arteritic Anterior Ischemic Optic Neuropathy Автор: Hayreh SS, Zimmerman MB (огляди 2020–2024) Журнал: Progress in Retinal and Eye Research Чому рання вазодилатація може посилювати пошкодження.
Книги та монографії
Glial Neurobiology: A Textbook (Verkhratsky A, Butt A, 2023) Глибоко про глію ЦНС та її роль у нейродегенеративних процесах, включаючи зоровий нерв.
Walsh & Hoyt’s Clinical Neuro-Ophthalmology: The Essentials (4th ed., 2021–оновлення 2024) Розділи про глію, NMOSD, MOGAD, NAION, glaucoma neuro-ophthalmic aspects.
Neuro-Ophthalmology: Diagnosis and Management (Kline LB, Bajandas FJ, 3rd ed., 2022) Дуже практичний посібник, з акцентом на діагностику та лікування.